Мамонов Василий Евгеньевич, к.м.н., научный руководитель отделения реконструктивно-восстановительной ортопедии для больных гемофилией, Гематологический научный центр РАМН;vasily-mamonov@yandex.ru
Ряшенцев Максим Маркович, к.м.н., старший научный сотрудник отделения реконструктивно-восстановительной ортопедии для больных гемофилией, Гематологический научный центр РАМН
Введение
Асептический некроз дистального эпифиза бедренной кости представляет собой медуллярный некроз, т.е. некроз элементов костного мозга, развивающийся вследствие тех или иных причин. В дальнейшем мы будем использовать словосочетание аваскуляный некроз (АВН), как наиболее устоявшееся в среде отечественных и зарубежных травматлогов-ортопедов (1, 6, 9, 21, 27, 30, 42, 43, 51, 63), хотя оно не всегда правильно отражает те процессы, которые происходят в костном мозге головки бедра и приводят к развитию типичных для этой патологии изменений.
АВН головки бедренной кости
АВН головки бедренной кости наблюдается в наиболее трудоспособном возрасте (3, 11, 16, 55). Заболевание до настоящего времени остаётся малоизученным разделом костной патологии. В последние годы интерес к нему заметно возрос, что объясняется следующим рядом факторов:
— увеличение частоты заболевания, которое нередко является главной причиной деформирующего коксартроза (28, 39);
— преимущественное поражение лиц молодого возраста (20-50 лет) (14, 20, 26);
— прогрессирующее течение заболевания с исходом в инвалидность (57, 44);
— частая двусторонняя локализация патологического процесса (37,7-80%) (5, 19, 49);
— низкая эффективность консервативного лечения;
— развитие метода эндопротезирования тазобедренного сустава, обеспечивающего быстрый и яркий клинический эффект, и возникновение целой отрасли медицинской индустрии, разрабатывающей и производящей эндопротезы.
В зависимости от причин, приводящих к АВН головки бедренной кости выделяют (12, 17, 22):
— алкогольный АВН — 20%
— кортикостероидный АВН — 35%
— идеопатический АВН — 45%.
В настоящем статье будут рассмотрены причины, приводящие к АВН головки бедра при заболеваниях системы крови. Здесь мы можем выделить токсический (преимущественно кортикостероидный), ишемический и инфильтративный механизмы развития АВН, которые имеют место, соответственно, при химиотерапии гематологических заболеваний, тромбофилии и болезнях накопления (7, 45).
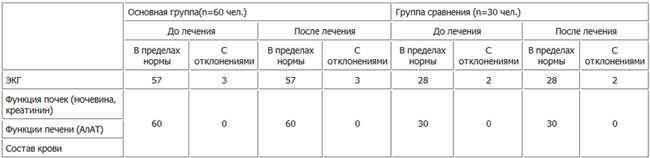
Таблица 1. Характеристика клинических проявлений АВН головки бедра при заболеваниях системы крови.
| Клинический признак |
Химиотерапия |
Болезнь Гоше |
Тромбофилии |
| Временная связь с токсическим воздействием |
+ |
— |
+/- |
| Связь с избыточной нагрузкой или травмой |
— |
— |
+ |
| Острое начало |
— |
— |
-/+ |
| Интенсивность болевого синдрома в дебюте АВН |
++ |
+++ |
+ |
| Эффективность консервативной терапии |
25% |
90% при дебюте АВН в детстве10% при дебюте АВН у взрослых |
30% |
АВН головки бедренной кости вследствие химиотерапии.
Во время проведения химиотерапии гемобластозов и при лечении иммунных, а иногда и апластических цитопений решающее влияние оказывает токсическое действие высоких доз глюкокортикостероидных гормонов. Этот механизм известен и подробно описан в литературе (9, 10, 23, 25, 58).
АВН, как правило, возникает у пациентов молодого возраста – 18-35 лет. Заболевание дебютирует остро, с появления интенсивного болевого синдрома в паховой области с иррадиацией дистально, до коленного сустава. Боли присутствуют как в покое, так и при осевой нагрузке. Болевой синдром, как правило, купируется приёмом нестероидных противовоспалительных препаратов. У большей части больных изменения наблюдаются и в других эпифизах длинных трубчатых костей – контрлатеральная головка бедра, проксимальный эпифиз плечевой кости, мыщелки бедренных костей. Часто поражение проксимального эпифиза бедра имеет тотальный или субтотальный характер. Появление болевого синдрома по времени связано с проведением химиотерапии, либо возникает на 2-4 недели позже.
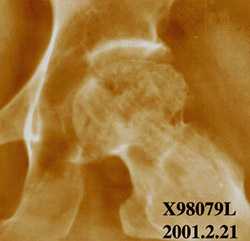
Принципиальное значение имеет ранняя диагностика АВН, которая заключается в выполнении МРТ тазобедренных суставов. Динамическое наблюдение процесса также осуществляется посредством МРТ не реже 1 раза в 3 месяца в течение первого года заболевания (12, 24, 31, 34).
Консервативная терапия направлена в первую очередь на профилактику развития АВН. Профилактическая терапия проводится во время проведения химиотерапии большими дозами глюкокортикостероидов и заключается в постоянном внутривенном введении гепарина, в амбулаторных условиях используются низкомолекулярные гепарины.
При выявлении АВН головки бедренной кости используется следующая схема лечения (16, 29, 62):
— разгрузка поражённого сустава – костыли, полупостельный режим;
— бисфосфанаты (золендроновая кислота и т.п.), при выраженном болевом синдроме перед назначением бисфосванатов в течение 1,5-3 месяцев проводится терапия миакальциком, который влияет на основную причину болей – повышенное внутрикостное давление;
— альфакальцидол в суточной дозе не менее 1 мкг;
— препараты кальция в суточной дозе 1-1,5 г.
При эффективности консервативного лечения через 12 месяцев, при переходе АВН в четвёртую стадию (по Рейнберг С.А.) назначается ЛФК, которая заключается в укреплении мышц бедра и тазового пояса, движениях в тазобедренном суставе без нагрузки весом тела. Консервативное лечение продолжается в течение двух лет. При возникновении укорочения поражённой конечности длина ног корректируется ортопедической обувью. ЛФК и элементы охранительного ортопедического режима продолжается пожизненно.
В случае преобладания остеолитических процессов, развитии клинически значимой дислокации бедра и укорочения конечности, а так же при болевом течении вторичного коксартроза этим пациентам показано тотальное эндопротезирование тазобедренного сустава.
АВН головки бедренной кости при болезнях накопления (на примере болезни Гоше).
Болезнь Гоше относится к болезням накопления липидов и обусловлена наследственным дефицитом фермента глюкоцереброзидазы (7, 18, 37). Накопление глюкоцереброзида в клетках моноцитарно-макрофагального ряда со временем приводит к инфильтрации ими органов-мишеней, к которым относится и костный мозг.
Одним из предрасполагающих факторов к развитию прогрессирующих костных поражений при болезни Гоше является спленэктомия (13, 36). Инфильтрация костного мозга клетками Гоше приводит к появлению медулярных некрозов, которые клинически проявляются костными кризами. 10-15% медуллярных некрозов при болезни Гоше локализуются в головке бедренной кости, приводя к развитию типичных для АВН проявлений (60).
Развитие АВН головки бедренной кости при болезни Гоше начинается с появления клиники «костного криза»: интенсивные (морфинные) боли, повышение температуры тела, ограничение функции тазобедренного сустава. Часто, клиника «костного криза» трактуется как остеомиелит, что влечёт за собой неоправданные хирургические вмешательства. Как правило, продолжительность «костного криза» не более 1-2-х недель. Симптомы регрессируют самостоятельно.
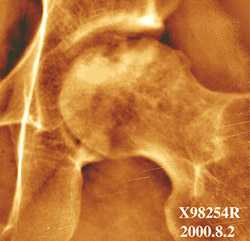
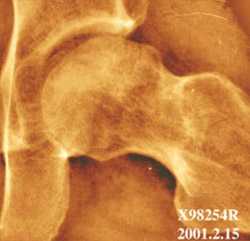
За время наблюдения за пациентами с болезнью Гоше и АВН головки бедренной кости нами была выявлена следующая закономерность. При дебюте АВН в детском возрасте преобладают процессы ремоделирования (32, 59). С ростом ребенка форма головки бедра изменяется, приобретая грибовидную деформацию, однако развития патологии суставного хряща, сужения суставной щели не происходит. Контуры головки бедра и вертлужной впадины приобретают конгруентность и во взрослом возрасте о наличии патологии тазобедренного сустава можно судить только по умеренному укорочению конечности (не более 2-х см) и некоторому уменьшению объёма движений в суставе. Боли в тазобедренном суставе не беспокоят даже при длительной физической нагрузке.
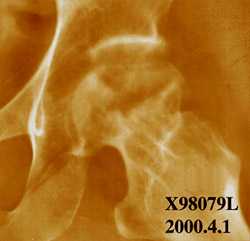
С другой стороны, если АВН головки бедра дебютирует у взрослого пациента с болезнью Гоше, даже локальное поражение сопровождается выраженным болевым синдромом и быстрым развитием вторичного коксартроза с нарушением функции тазобедренного сустава (59).
Консервативная терапия медуллярного некроза проксимального эпифиза бедренной кости при болезни Гоше заключается в следующем:
— назначение ферментной заместительной терапии (Церезим);
— охранительный ортопедический режим, разгрузка поражённой конечности;
— бисфосфанаты;
— альфакальцидол;
— препараты кальция;
— ЛФК.
У взрослых пациентов, перенёсших АВН головки бедра в детском возрасте, лечение ограничивается лечебной физкультурой и назначением хондропротекторов при появлении признаков коксартроза (8, 33).
Консервативная терапия при развитии АВН головки бедра во взрослом возрасте имеет эффективность не более 10%. При неэффективности терапии в течение года определяются показания к тотальному эндопротезированию тазобедренного сустава.
АВН головки бедренной кости при тромбофилиях.
Тромбофилии – группа патологических состояний, определяющих склонность к развитию тромботических осложнений. Выделяют наследственную, приобретённую и комбинированную тромбофилии.
Наследственная тромбофилия подразумевает наличие у больного генетической мутации, повышающий риск развития тромбозов, т.н. тромботический диатез. Наследственная тромбофилия проявляется во взрослом возрасте и, как правило, в сочетании с другими факторами, способствующими гиперкоагуляции крови.
Приобретённая тромбофилия — патологическое состояние, приводящее к тромботическим осложнениям, у пациентов, страдающих аутоиммунными (антифосфолипидный синдром), онкологическими или хроническими инфекционными процессами.
Сочетание наследственной предрасположенности с приобретённой тромбофилией (комбинированная тромбофилия) резко повышает риск возникновения тромбозов.
Тромбофилия играет одну из ведущих ролей в развитии АВН головки бедренной кости у пациентов, имеющих наследственную предрасположенность, или выше указанную соматическую патологию (4, 46). Провоцирующим фактором может служить травма или избыточная физическая нагрузка, а так же хроническая интоксикация (например, алкогольная). Ведущим механизмом в развитии АВН у пациентов с тромбофилией является тромбоз венозных коллекторов эпифиза.
Клинически АВН при тромбофилии проявляется болями, которые характеризуются неопределённой локализацией и склонностью к широкой иррадиации: в область поясницы и ягодицы, голени; в паховую область, а особенно часто (до 70% случаев) — в область коленного сустава (4, 60). Именно эти отдалённые болевые ощущения воспринимаются как основные и легко уводят от правильного диагноза. Вначале боли малоинтенсивны, появляются при ходьбе, плохой погоде и исчезают в покое, постепенно становятся постоянными и более интенсивными, усиливаясь при нагрузке. После периода обострений порой наступает облегчение, но затем симптомы заболевания нарастают. В ряде случаев начало заболевания может быть внезапным. Одним из наиболее ранних симптомов заболевания — ограничения ротационных движении бедра, особенно внутренней ротации (80-85% случаев), сопровождающееся болевым синдромом. Затем отмечается ограничение отведения, а в последнюю очередь уменьшение подвижности в сагиттальной плоскости.
Морфологически при АВН головки бедренной кости на фоне тромбофилии преобладают локальные поражения, чаще – в зоне максимальной нагрузки.
Консервативная терапия направлена на коррекцию коагуляционных нарушений и профилактику тромботических осложнений в зависимости от типа тромбофилии (2, 15):
— дискретный малообъёмный плазмаферез;
— прямые и непрямые антикоагулянты;
— препараты, улучшающие реологию крови;
— витаминотерапия при некоторых формах наследственной тромбофилии (дефекте гена метилентетрагидрофолат редуктазы).
Помимо терапии коагуляционных нарушений стандартно применяется охранительный ортопедический режим, терапия бисфосфонатами, альфакальцидолом и препаратами кальция описанная выше. Лечебная физкультура применяется на четвёртой стадии процесса при развитии вторичного коксартроза.
У пациентов с тромбофилией консервативное лечение в 30% случаев позволяет получить хороший клинический эффект. Показанием к операции служит выраженный болевой синдром, связанный с развитием вторичного коксартроза, а так же значительная дислокация бедра с укорочением конечности и разрушением крыши вертлужной впадины (35, 56).
Риски, связанные с хирургическим лечением АВН головки бедренной кости при заболеваниях системы крови.
При заболеваниях системы крови риск развития осложнений, связанных с хирургическим лечением, значительно выше, чем в общей популяции пациентов с АВН головки бедренной кости (38, 61).
Геморрагические осложнения связаны с гипокоагуляционными нарушения гемостаза:
— патология тромбоцитарного звена гемостаза – имеет место при болезни Гоше, апластической и иммунной тромбоцитопении;
— патология сосудистого и плазменного гемостаза встречается при антифосфолипидном синдроме, дефиците факторов свёртывания крови, синтезируемых в печени, при болезнях накопления.
Кровотечения во время операции и в раннем послеоперационном периоде могут иметь фатальный характер, вызывать вторичные нарушения гемостаза в виде ДВС синдрома, приводить к гибели больного.
Тромбофилии так же могут быть причиной развития геморрагического синдрома во время операции и раннем послеоперационном периоде вследствие развития коагулопатии потребления и ДВС синдрома (48, 53, 54).
Наличие у пациентов тромбофилии является основной причиной развития тромботических и тромбоэмболических осложнений в послеоперационном периоде, часто сводящих на нет все усилия хирургов. Профилактика тромботических осложнений в периоперационном периоде у пациентов с тромбофилией на сегодняшний день остаётся сложной и окончательно не решённой задачей (41, 45).
Кроме кровотечений и тромбозов при эндопротезировании тазобедреного сустава у пациентов с заболеваниями системы крови, перенесших химиотерапевтическое лечение или получающих иммуносупрессивную терапию (в том числе и глюкокортикоидными гормонами), а так же при болезнях накопления значительно повышается риск инфекционных осложнений и появление ранней нестабильности компонентов эндопротеза (40, 50, 52, 54).
Таблица 2. Осложнения хирургического лечения АВН головки бедра при заболеваниях системы крови.
| Осложнение |
Тромбоцитопении |
Болезнь Гоше |
Тромбофилии |
| Кровотечение |
+ |
+ |
+/- |
| Тромбозы, ТЭЛА |
— |
+/- |
+ |
| Инфекционные осложнения |
+ |
+ |
— |
| Ранняя нестабильность эндопротеза |
+ |
+ |
— |
Выводы.
- Показанием к эндопротезированию у гематологических больных служит стойкий выраженный болевой синдром вследствие прогрессирующего остеолизиса или вторичного коксартроза, а также прогрессирующая дислокация бедренной кости, приводящая к инвалидизации пациентов.
- Необходимо максимально использовать возможности консервативного лечения АВН головки бедренной кости у пациентов с заболеваниями системы крови.
- Эндопротезирование тазобедренного сустава при АВН головки бедренной кости у гематологических больных должно производиться в специализированном стационаре, связано с серьёзными рисками и требует больших финансовых затрат.
Литература:
1. Abderhalden R. Fruherfassung der Huftgelenksdysplasie imNeugeborenenalter / R. Abderhalden, M. Amato // Nestle Wissenschaftlicher Dienst.- Munchen, 1995.- 55 s.
2. Arie E. Femofal head shape in Perthes disease: Is the contralateral hip abdominal / E. Arie, F. Johnson, M. H. Harrison // Clin. Orthop.-1986.- N 209.- P. 77-88.
3. Arlet J. Diagnostie de l’osteonecrose femur capitale au syade I / J. Arlet, P. Ficat // Rev. Chir. Orthop.- 1968.-V. 54, N 7.- P. 637-656.
4. Arlet J. Necrose tt ischemie de la tete femoral au cours des members inferieurs enquete sur 138 ateritques et 159 aortographies / J. Arlet, J. P. Millet, A. Gedean // Rev. Rheum.- 1975.-V. 42.- P. 391-396.
5. Axhausen G. Ueber anaemische infarct am Knochensystem und ihre Bedeutung fuer die Lehre von den primaren Epiphyseonecrosen / G. Аxhausen // Archy. klin.Chir. – 1928.- Bd 151.- S. 72.
6. Barker D. J. P., Hall A. J. The Epidemiology of Perthes disease / D. J. P. Barker, A. J. Hall // Clin. Orthop.- 1986.-V. 209.- P. 89-94.
7. Batory I. Die Aetiologie des Morbus Perthes und sein Besiehung zu der Dysplasia Capitis Femoris / I. Batory // Z. Ortop.-1982.- Bd. 120, N 6.- S. 833-849.
8. Batory I. Opinions and comparative observations about the etiology of Legg-Calve –Perthes disease / I. Batory // Arch. Orthop. Traum. Surg.- 1982.- V.100, N 3.- P. 151-162.
9. Bruns J. Verbesserte Fruhdiagnostik der Femurkopfosteonecrose / J. Bruns, M.Heller, J.Knop et al. // Chir.Praxis.-1987/88.- Bd. 38.- P. 693-700.
10. Burwell R. G. Editorial comment / R. G. Burwell, M. H. Harrison // Clin.Orthop.- 1986.- N 209.- P. 2-4.
11. Calve J. Sur une particuliere forme de pseudo-coxalgie greffee sur deformations caracteristiques de l’extrerite superieure du femur / J. Calve // Rev. Chir., 1910. — V. 42.- P. 54-84.
12. Catteral A. Natural history, classification and X-ray sings in Legg-Calve-Perthes’ disease / A. Catteral // Acta orthop. Belg.- 1980.- V.46, N 4.-P. 346-351.
13. Clanton Th. O. Osteochondritis dissecans. History, pathophysiologic and current treatment concepts. / Th. O. Clanton, J. S. De Lee // Clin. Orthop.- 1982.- N 167.- P. 50-64.
14. Coleman S. Femoral neck fracture: pathogenesis of avascular necrosis nonunion and late degenerative changes / S. Coleman, C. Compere // Clin.orthop.- 1961.- N 20.- P. 247-252.
15. Coleman B.J. Radiografically negative avascular necrosis: detection with MR imaging / B. J. Coleman, H. Y. Kressel, M. K. Dalinke // Radiology.- 1988.-V. 168, N 1.-P.30-39.
16. Cruess R. L. Osteonecroses of bone: Current concept as to etiology and pathogenesis / R. L. Cruess // Clin. Ortop. – 1986. – N 208.- P. 30-39.
17. Chung S.M.K. The arterial supply of the developing proximal end of the human femur / S. M. K. Chung // J. Bone Jt. Surgery.- 1976.- V. 58-A, N 7.- P. 961-970.
18. Doria A. S. Three – Dementional (3D) contrast – enhanced power Doppler imaging in Legg – Calve – Perthes disease / A. S. Doria, R. Guarniero, F. G. Cunha // Pediatr. Radiol.- 2000.- N 12.- V. 30.- P. 871-874.
19. Doria A.S. Contrast – enhanced power Doppler sonography: assessment of revascularization flou in Legg – Calve – Perthes disease / A. S. Doria R. Guarniero, F. G. Cunha, M. Modena // Ultrasound med. Biol.- 2002.- V. 28, N 2.- P. 171-182.
20. Doria A. S. Contrast – enhanced power Doppler imaging: comparison with scintigraphic phases of revascularization of the femoral head in Legg– Calve – Perthes disease / A. S. Doria, R. Guarniero, F. G. Cunha // Petadydiatr. Orthop. 2002.-V. 22.- N 4.- P. 471-478.
21. EFSUMB Newsletter.- 1996.- Issue 2.-V.2.
22. Ferguson A. B. Synovitis of the hip and Legg- Perthese disease / A.B. Ferguson // Clin. Orthop.- 1954.- N 4.- P. 180-188.
23. Ferguson A.B. Recent advances in understanding Legg-Perthes disease / A.B. Ferguson // Orthop. Survey.- 1978.-V.1, N 4.- P. 307.
24. Ficat P. Arthrose et necrose / P. Ficat // Rev. Chir.- 1974.- V. 60.- P. 123-133.
25. Ficat R.P. Early diagnosis of osteonecrosis by functional bone investigation / R.P. Ficat // Progress in orthopaedics surgery.- 1981.- V. 5.- P. 17-27.
26. Frasez P. Further experience with discriminant functions in differential diagnosis of hypercalcaemia / P. Frasez, M. Healy, L. Watson // Postgrad. Med.- 1976.- V. 52.- P. 254-257.
27. Genes B. M. Early osteonecrosis of the femoral head: detection in high-risk patients wish MR imaging / B. M. Genes, M. R. Wilson, R. W. Houk // Radiology.- 1988.-V. 168, N 2.- P. 521-524.
28. Gill T.J. Intraoperative assessment of femoral head vascularity after femoral neck fracture / T. J.Gill, J. B. Sledge, A. Ekkernkamp // J. Orthop. Trauma. — 1998.-V. 12., N 7.- P. 474-478.
29. Graf R. The diagnosis of congenital hip joint dislocation by the ultrasonic compound treatment / R. Graf // Arch. Orthop. Trauma Surg.- 1980.- V. 97.- P. 117-133.
30. Graf R. Fundamentals of sonographic diagnosis of infant displasia / R. Graf // Pediatr. Orthop. — 1984.- N 4.- P. 735-740.
31. Green N. E. Intraosseous venous pressure in Legg-Calve-Perthes disease / N. E. Green, P. P. Griffin // J.Bone Jt. Surgery.- 1982.-V. 64-A, N 5.- P. 666-671.
32. Harland U. Ultraschallfibel Orthopadie Traumatologie Rheumatologie / U. Harland, H. Salter // Springer-Verlag Berlin etc.- P. 184.
33. Harrison M. H. M. A preliminary account of the management of the painful hip originating from Perthes disease // Clin.orthop.- 1986.- N. 209.- P. 57-64.
34. Harrison M. H. M. Perthes disease treatment with the Birmingham splint / M. N. M. Harrison, Turner M. H., Smith D. N. // J. Bone Jt. Surg.- 1982.- V. 64-B, N 1.- P. 3-11.
35. Hasegawa G. Scintimetry in transient synovitis of the hip in the child / G. Hasegawa, H. Windstrand, T. Gustavson // Acta Oprthop. Scand.- 1988.- V. 59, N 5.- P. 520-525.
36. Hesse B. Does it always have to be Perthes disease? What is epiphiseal dysplasia ? / B. Hesse, G. Kohler // Clin. Orthop.- 2003.- Vol. 414.- P. 219-227.
37. Higer H. P. Transistoriche Osteoporose oder Femurkopfnecrose? Fruhdiagnose mit der MRT / H. P. Higer, J.Grimm, P.Pedrosa // Fortsch. Rontgenstr.- 1989.- Bd. 150, H. 4.- S. 407-412.
38. Hulth A. Necrosis of the head of the femur / A. Hulth // Acta Chir. Scand.- 1961.- V. 122, N 1.- P. 75-84.
39. Ingman A. M. A comparison between innominate osteotomy and hip spica in the treatment of the Legg- Calve- Perthes disease / A. M. Ingman, D. C. Peterson, A.D. Sutherland // Clin.Orthop.- 1982.- N. 163.- P. 141-147.
40. Jacobs B. Epidemiology of traumatic and nontraumatic osteonecrosis / B. Jacobs // Clin. Orthop.- 1978.- N. 130.- P. 51-68.
41. Joseph B. Natural evolution of Perthes disease: a stady of 610 children under 12 jears of age at disease onset / B. Joseph, G. Varghese, K. Mulpuri // Pediatr. Orthop.- 2003. -V. 23. — N 5.- P. 590-600.
42. Kayser R. Value of ultrasound diagnosis in Legg — Calve – Perthes disease / R. Kaiser, J. Franke, K. Mahlfeld // Scweiz. Rudsch. Med. Prax. – 2003.-V. 99, N 24.- P. 1123-1127.
43. Klisic P. J. Perthes disease / P. J. Klisic // Int. Orthop.- 1984.-V. 8.- P. 95-102.
44. Landin L. A. Transient synovitis of the hip. Its incidence, epidemiology and relation to Perthes disease / L. A. Landin, L. C. Danielsson, C. Wattagard //J. Bone Jt. Surgery.- 1987.- V. 69-B, N 2.- P.238-242.
45. Lausten G. S. Blood perfusion uneven in femoral head osteonecrosis / G. S. Lausten, C. C. Arnoldi // Acta Orthop. Scand.- 1993.-V.64, N 5.- P. 531-533.
46. Lecuire F. Evolution a long-term de la hanche (Legg-Calve-Perthes) / F. Lecuire, J. Rebouillat // Rev. Chir. Orthop.- 1987.- V. 73.- P. 561-569.
47. Legg A. T. An obscure affection of the hip-joint / A. T. Legg // Boston Med. Surg. J.- 1910.- N 162.- P.202-204.
48. Moitrelli G.Osteonecrosis of the hip treated by intertrochanteric osteotomy / G.Moitrelli, V. Fusco, A.Avai // J. Bone Jt. Surgery.- 1988.- V. 70-B, N 5.- P. 761-766.
49. Nochimson Georgy Legg — Calve – Perthes Disease. (Medline)
50. Orhoseek Meesege Forum. Legg — Calve – Perthes Disease. (Medline)
51. Orler R. Avascular femur head necrosis as severe complication after femoral intramedullary nailing in children and adolescents / R. Orler, O. Hershe, D. L. Helfet // Unfallchirurg.- 1998.- Bd. 101, H. 6.- S. 495-499.
52. Perthes G. Uber Arthritis deformans juvenilis / G. Perthes // Dtsch. Z. Chir.- 1910.- V. 107., N 1-3.- S. 111-159.
53. Portigliatty Barbos M. The biology of idiopathic necrosis of the human femoral head studied by tetracycline labeling and microcardiography / M. Barbos Portigliatty, F. Mica Botto, F. Denicolai // Acta Orthop. Belg.- 1985.-V. 51, N 1.- P.18-27.
54. Salter R.B. The prognostic significanse of the subhondrial frachture and a two-group classification of the femoral head involvement / R. B. Salter, G. H. Thomson // J. Bone Jt. Surg.- 1984.-V. 66-B, N 4.- P. 479-489.
55. Schulz R. D. The present of ultrasonography in newborn and young infants hips / R. D. Schulz, M. Zieger // Ann. Radiol.- 1986.-V. 29.- N 8.- P.681-685.
56. Simon G. F. Robben Anterior Joint Capsule of the normal Hip and in Children wish Transient Sinovinis: US Stady with Anatomic and Histologic Correlation / Simon G.F. Robben, Maarten H. Lequin, Ad F.M. Diepstrated // Radiology. – 1999.- V. 210.- P. 499-507.
57. Standard for real-time Display of Thermal and Mechanical Acoustic Output Indices on Diagnostic Ultrasound Equipment // Rockville, Maryland, AIUM/NEMA.- 1992.
58. Starclint H. Microvascular obstruction in avascular necrosis / H. Starclint, G.S. Lausten, C.C. Arnoldi // Acta Orthop. Scand.- 1995.- V. 66, N 1.- P. 9-12.
59. Steib J. P. Etude par microspheres radioactives de la microcirculation osseuse dans l’osteonecrose aseptique de la tete femorale / J. P. Steib, B. Moyses, J. J. Wenger // Rev. Chir. Orthop.- 1987.- V. 73, N. 8.- P. 601-608.
60. Weiland A. J. Vascularized bone autografts. Experience with a case / A. J. Weiland, J. R. Moore, R. K. Daniel // Clin. Orthop.- 1983.- N 174.- P. 87-95.
61. Welfling J. Embolies micro-particularies et necrose de la tete femorale chez l’adulte / J. Welfling // Rev. Rheum.- 1967.- V. 3, N 2.- P. 126-130.
62. Wells P. N. T. Physical and technical aspects of colour flouw ultrasound / P.N.T. Wells // Diagnostic Vascular Ultrasound Ed. By Labs K. H. L.- Edward Arnold, 1992.- P. 145-153.
63. Wirth T. Ultrasonography in Legg — Calve – Perthes disease / T. Wirth, G. W. LeQuesne, D. S. Paterson // Pediatr. Radiol. 1993.-V. 23.- N 4.- P. 331-332